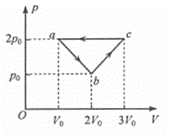
一定质量的理想气体从状态a开始,经a→b、b→c、c→a三个过程后回到初始状态a,其p-V图像如图所示。已知三个状态的坐标分别为a(V0, 2p0)、 b(2V0,p0)、c(3V0,2p0) 以下判断正确的是( )
A.气体在a→b过程中对外界做的功小于在b→c过程中对外界做的功
B.气体在a→b过程中从外界吸收的热量大于在b→c过程中从外界吸收的热量
C.在c→a过程中,外界对气体做的功小于气体向外界放出的热量
D.气体在c→a过程中内能的减少量大于b→c过程中内能的增加量
答案
C
【解析】
A.根据气体做功的表达式![]() 可知
可知![]() 图线和体积横轴围成的面积即为做功大小,所以气体在
图线和体积横轴围成的面积即为做功大小,所以气体在![]() 过程中对外界做的功等于
过程中对外界做的功等于![]() 过程中对外界做的功,A错误;
过程中对外界做的功,A错误;
B.气体从![]() ,满足玻意尔定律
,满足玻意尔定律![]() ,所以
,所以
![]()
所以![]() ,根据热力学第一定律
,根据热力学第一定律![]() 可知
可知
![]()
气体从![]() ,温度升高,所以
,温度升高,所以![]() ,根据热力学第一定律可知
,根据热力学第一定律可知
![]()
结合A选项可知
![]()
所以
![]()
![]() 过程气体吸收的热量大于
过程气体吸收的热量大于![]() 过程吸收的热量,B错误;
过程吸收的热量,B错误;
C.气体从![]() ,温度降低,所以
,温度降低,所以![]() ,气体体积减小,外界对气体做功,所以
,气体体积减小,外界对气体做功,所以![]() ,根据热力学第一定律可知
,根据热力学第一定律可知![]() ,放出热量,C正确;
,放出热量,C正确;
D.理想气体的内能只与温度有关,根据![]() 可知从
可知从
![]()
所以气体从![]() 过程中内能的减少量等于
过程中内能的减少量等于![]() 过程中内能的增加量,D错误。
过程中内能的增加量,D错误。
故选C。

 分析
分析 

 ,等温降压膨胀,内能不变,吸热等于对外做的功。
,等温降压膨胀,内能不变,吸热等于对外做的功。  ,等容升温升压,不做功,吸热等于内能增加。
,等容升温升压,不做功,吸热等于内能增加。  ,等压降温压缩,放热等于外界做功和内能减少量。
,等压降温压缩,放热等于外界做功和内能减少量。  。
。 状态及能量变化同等温线分析。
状态及能量变化同等温线分析。 
 等温升压压缩,内能不变,外界做功等于放热;
等温升压压缩,内能不变,外界做功等于放热; 等压升温膨胀,吸热等于内能增加量和对外做的功;
等压升温膨胀,吸热等于内能增加量和对外做的功; 等容降温降压,内能减小量等于放热。
等容降温降压,内能减小量等于放热。
